Полиэтилен - очень распространённый в промышленности и быту полимер, получаемый методом полимеризации Этилена. С обычным полиэтиленом ассоциируется множество предметов обихода. Популярность полиэтилену придали его дешевизна и выдающиеся химические и физические свойства. Он не дорог в производстве, нетоксичен, физиологически инертен, легко обрабатывается, водонепроницаем, имеет высокую химическую стойкость, практически не корродирует, обладает приемлемой механической и отличной диэлектрической прочностью и т.д. Неудивительно, что полиэтилен занимает первое место в мире по объёмам производства среди всех органических веществ! Для дополнительного улучшения физических свойств полиэтилена и расширения сферы его применения учённые придумали технологию, называемую "сшивкой".
"Сшивкой" полиэтилена называют физический процесс, который модифицирует внутреннюю молекулярную структуру материала без изменения химического состава вещества. Делается это для того, чтобы придать материалу новые, полезные физические свойства, позволяющие существенно расширить сферы его применения.
Говоря сухим научным языком, сшивка полиэтилена - это процесс связки звеньев его молекул в широкоячеистую трехмерную сетку, путём образования поперечных связей. Звучит непонятно? На самом деле всё просто, давайте рассмотрим этот процесс подробнее.
Рис. 1. Молекула этилена
Из школьного курса химии мы помним, что все вещества состоят из атомов, которые, в свою очередь, группируются в молекулы. От того, насколько прочной будет связь между атомами, напрямую зависят свойства вещества. Будет ли оно твёрдым, жидким или газообразным, будет ли оно активно вступать в химические реакции или будет стабильным (инертным, химичеки неактивным), будет ли оно гореть и т.д. - всё зависит от прочности и структуры химических связей между атомами вещества.
Для того, чтобы понять физико-химические процессы, происходящие при сшивке полиэтилена, необходимо напомнить, что такое полимеры и как они образуются. Рассмотрим простое органическое вещество: Этилен (C2H4). Этилен представляет из себя бесцветный горючий газ со слабым запахом. Его молекула состоит из двух атомов углерода (C) и двух атомов водорода (H). Углерод в молекуле этилена способен образовывать четыре прочные химические связи, а водород только одну (химические связи между атомами принято обозначать штрихами). Молекула Этилена самодостаточна, она не имеет свободных атомов, все химические связи находятся "при деле". У этилена наиболее крепкой является связь между атомами углерода, так как она двойная, а связи углерода с водородом не очень прочны. Двойная связь между атомами углерода тоже имеет особенности: одна из связей менее крепкая чем другая. Запомним эту особенность, она нам чуть позже понадобится.
Чтобы разорвать любую химическую связь между атомами нужно преодолеть силу межатомного притяжения. Сделать это можно с помощью дополнительной энергии, сообщённой (переданной) атомам, при чём эта энергия должна быть больше, чем энергия межатомного взаимодействия. И не важно, каким путём (химическим или физическим) будет осуществляться воздействие. Главное - чтобы оно было достаточным! Нагрев - простейший пример сообщения веществу дополнительной энергии. Именно поэтому многие химические реакции протекают только при высоких температурах.
В случае с этиленом одного нагрева оказывается недостаточно, но существует ряд других способов, позволяющих частично разорвать двойную связь между атомами углерода, вытягивая молекулу этилена в двухзвенную цепочку. Каждое звено этой цепочки называют мономером, от греческого слова "монос" - один и "мерос" - часть. Почему мы говорим о частичном разрыве? Потому что фактически из двух связей разрывается только одна, менее прочная. А дальше начинает происходить интересное: каждая из этих полуразорванных молекул, обладая двумя свободными и готовыми для соединения химическими связями стремится их задействовать. При этом мономеры начинают соединяться друг с другом последовательно, образуя своеобразную бесконечную цепочку, превращаясь по сути в одну макромолекулу, которую и называют полимером (от греческого "Поли" - много и "мерос" - часть). Похожим образом образуются и другие полимеры (полипропилен, поливинилхлорид, политетрофторэтилен и т.д.) цепочки которых могут иметь схожее или более сложное строение.
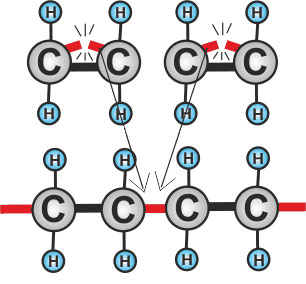
Рис. 2. Превращение этилена в полиэтилен
Наконец мы дошли и до самой сшивки. Сшивка полиэтилена - ни что иное, как способ соединения отдельных цепочек полимера между собой. Если после полимеризации мы получаем как-бы отдельные нити вещества, то с помощью сшивки мы соединяем эти нити в сеть. Понятно, что любая ткань гораздо прочнее отдельных ниток, из которых она состоит, поэтому сшитый полиэтилен становится более прочным и тугоплавким и способен выдержать более высокую температуру, чем его обычный, несшитый аналог.
Для осуществления процесса сшивки необходимо разорвать некоторые второстепенные межатомные связи у каждой цепочки и использовать их затем для соединения цепочек между собой. Сделать это можно разными способами, но все они делятся на два вида: физический и химический. Заметим, что при воздействии на полиэтилен легче всего разрываются менее прочные химические связи, каковыми являются связи между углеродом и водородом. При этом связь углерод-углерод, как более прочная остаётся целой и сама полимерная цепочка при сшивке не повреждается.
Наконец мы дошли и до самой сшивки. Сшивка полиэтилена - ни что иное, как способ соединения отдельных цепочек полимера между собой. Если после полимеризации мы получаем как-бы отдельные нити вещества, то с помощью сшивки мы соединяем эти нити в сеть. Понятно, что любая ткань гораздо прочнее отдельных ниток, из которых она состоит, поэтому сшитый полиэтилен становится более прочным и тугоплавким и способен выдержать более высокую температуру, чем его обычный, несшитый аналог.
Для осуществления процесса сшивки необходимо разорвать некоторые второстепенные межатомные связи у каждой цепочки и использовать их затем для соединения цепочек между собой. Сделать это можно разными способами, но все они делятся на два вида: физический и химический. Заметим, что при воздействии на полиэтилен легче всего разрываются менее прочные химические связи, каковыми являются связи между углеродом и водородом. При этом связь углерод-углерод, как более прочная остаётся целой и сама полимерная цепочка при сшивке не повреждается.
При облучении полиэтилена потоком высокоэнергетических заряженных частиц (рентгеновское или гамма излучение), генерируемых специальным акселератором (ускорителем), некоторые атомы водорода отщепляются от полимерных цепочек. Нескомпенсированные свободные связи атомов углерода тут же стремятся вновь вступить в реакцию, но уже не с водородом, а друг с другом, "сшиваясь", образуя между собой дополнительную прочную связь. "Лишние" атомы водорода так же взаимодействуют между собой, выделяясь в видемолекулярного водорода (H2).
В результате появляется прочная трёхмерная сеть из полимерных цепочек этилена. Вещество как бы переходит из аморфного состояния в кристаллическое, ведь упорядоченную сетчатую структуру сшитого полиэтилена вполне можно сравнить с кристаллической решеткой многих твёрдых веществ. Вот почему этот процесс называется поперечной сшивкой полиэтилена, хотя иногда встречается и другие термины: модифицированный полиэтилен, радиационно-модифицированный полиэтилен, радиационно-сшитый полиэтилен и т.д.
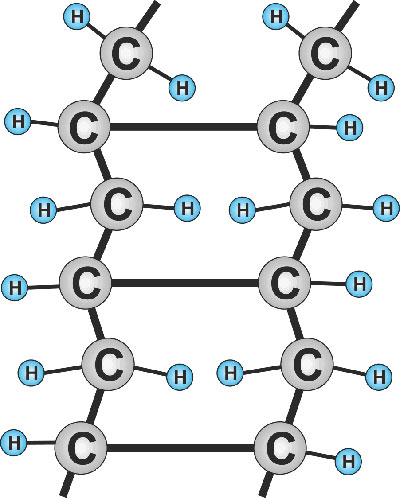
Рис. 3. Сшитый полиэтилен
После сшивки, кроме увеличения температуры полавления, материал приобретает ещё одно ценное свойство - "память" формы, так как из аморфного куска пластассы он превращается в вещество с чёткой структурой внутри. Растягивая подогретый модифицированный полиэтилен мы нарушаем внутреннее равновесие в его вновь образованных химических связях, вызывая упругие напряжения в его структуре. После охлаждения полиэтилен застывает, сохраняя свою новую форму. Но лишь только его снова нагреют, полиэтилен стремится вернуться в первоначальное, равновесное состояние, в котором межмолекулярные связи чувствуют себя наиболее комфортно. Здесь будет уместна аналогия с детскими качелями. Представьте, что Вы сильно отклонили качели сторону и мгновенно заморозили их в куске льда. Лишь только лёд растает, качели вернутся в своё естественное положение.
Без сшитого полиэтилена или полипропилена сейчас невозможно представить полимерные водонапорные водопроводные трубы, которые пришли на смену ржавеющим железным. С холодной водой всё понятно, но вот горячую воду труба из обычного полиэтилена долго выдержать не может - расплавится! А сшитому эта задача вполне по плечу!